近日,我校寒地心血管病全国重点实验室季勇教授团队在国际权威期刊Science Translational Medicine上发表题为《S-nitrosoglutathione reductase as a therapeutic target for diabetic vascular complications in rodent models》的研究论文。该研究首次揭示亚硝基谷胱甘肽还原酶(GSNOR)通过非酶活依赖的方式参与糖尿病血管并发症的新机制,并创新性研发了口服小分子化合物NYY-001,可通过靶向GSNOR改善糖尿病血管内皮功能障碍。该研究不仅为理解糖尿病血管并发症的分子机制提供了新视角,也为临床治疗提供了具有转化潜力的新候选药物。

糖尿病是严重危害人类健康的公共卫生问题,糖尿病引起的各类血管并发症是导致患者致死、致残的主要原因,临床上单一的降糖治疗并不能完全消除糖尿病患者各类血管并发症的发生风险,因此深入理解糖尿病血管并发症的发病机理并寻找潜在干预手段,开发联合治疗策略,对于临床干预具有重要意义。
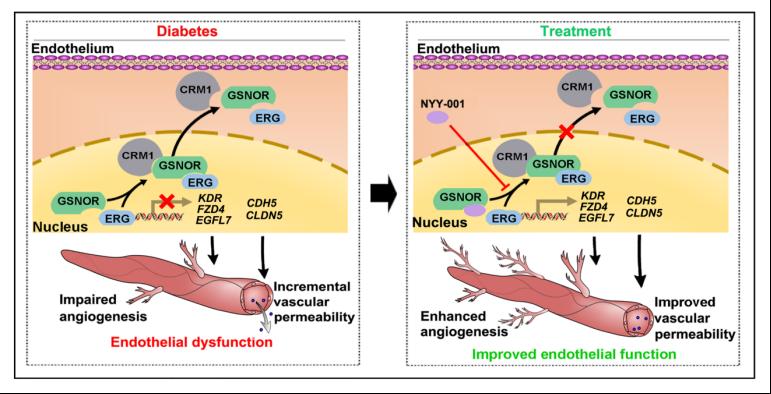
GSNOR是亚硝基谷胱甘肽(GSNO)代谢的关键酶,在调控细胞内一氧化氮和蛋白质巯基亚硝基化修饰的稳态平衡中发挥关键作用,但是其在糖尿病血管内皮功能障碍中的作用尚未明确。本研究通过蛋白质组学筛选发现,GSNOR在糖尿病患者及糖尿病模型动物的血管内皮细胞中表达显著升高。而内皮细胞特异性敲除GSNOR可促进糖尿病小鼠缺血侧肢的血流恢复和血管新生,并改善血管通透性和舒张功能。进一步机制研究表明,GSNOR通过核输出蛋白CRM1依赖的通路,介导转录因子ERG的出核转运,进而抑制ERG下游血管稳态相关基因的表达,从而导致血管内皮功能障碍。该作用不依赖于GSNOR的酶活功能,基于该机制,研究团队设计并合成了全新的小分子化合物—NYY-001,该化合物具备良好的口服吸收效果和安全性,可有效阻断GSNOR与ERG的结合,促进糖尿病小鼠缺血下肢的血流恢复和血管新生情况,并改善血管通透性。
季勇教授团队长期致力于GSNOR在心血管疾病中的作用研究,取得了一系列重大发现。团队前期研究揭示了GSNOR在心脏重构中的关键调控作用:首次阐明GSNOR通过调控LIM结构域肌蛋白(MLP)和热休克蛋白90(HSP90)的巯基亚硝基化修饰,参与病理性心肌肥厚(Circulation. 2020;141(12):984-1000; Acta Pharmacol Sin. 2022;43(8):1979-1988);进一步发现E3泛素酶NEDD4介导的GSNOR泛素化降解在病理性心肌肥厚中发挥关键调控作用(Circ Res. 2025;136(4):422-438);此外,团队首次报道了GSNOR定位于心肌细胞线粒体,并通过调控腺嘌呤核苷酸转位酶1(ANT1)的巯基亚硝基化修饰参与心力衰竭(Circ Res. 2023;133(3):220-236)。在此基础上,本研究进一步取得突破性进展,首次揭示GSNOR以非酶活依赖的全新方式,在糖尿病血管重构中发挥核心作用。这一发现不仅拓展了GSNOR的生物学功能认知,更为全面阐释其在心血管疾病中的多重角色提供了关键科学依据。该研究从全新视角解析了糖尿病血管并发症的分子机制,为临床干预提供了具有重要转化价值的新策略。
我校寒地心血管病全国重点实验室季勇教授、南京医科大学谢利平教授、哈尔滨医科大学附属第二医院韩艺教授为该论文的共同通讯作者。南京医科大学赵爽副教授、宋天宇博士、唐欣副教授为该论文共同第一作者。该研究获得国家自然科学基金创新研究群体项目、国家自然科学基金专项项目、国家重点研发计划等项目资助。该工作得到了中国人民解放军北部战区总医院韩雅玲院士、闫承慧教授,南京医科大学陈峰教授、陈宏山教授、殷国勇教授、王连生教授、高原青教授,南京大学医学院附属鼓楼医院王东进教授,Temple University王虹教授,上海交通大学医曹禹教授,中国科学院遗传与发育生物学研究所王秀杰教授,哈尔滨医科大学于波教授、张志仁教授的大力支持。
原文链接:https://www.science.org/doi/10.1126/scitranslmed.adn9216