近日,哈尔滨医科大学基础医学院王广友教授、张彤帅副教授团队与第一临床医学院神经内科等人合作,在《FASEB Journal》期刊(JCR Q1/中国科学院2区)发表题为“The CCL11-CCR3 Axis Regulates the Aggravation of Neuroinflammation in Astrocytic Necroptosis After Cerebral Ischemia”的研究论文。该研究首次揭示了趋化因子CCL11及其受体CCR3在脑缺血后星形胶质细胞坏死性凋亡中的关键调控作用,并阐明了该信号轴如何通过激活RIPK1/RIPK3/MLKL通路加剧神经炎症反应,进而加重神经元损伤。该研究为缺血性脑卒中的病理机制提供了全新视角,并为临床干预提供了潜在新靶点。

研究发现,在脑缺血损伤早期,趋化因子CCL11表达显著上调,并通过结合星形胶质细胞表面的CCR3受体,激活坏死性凋亡信号通路,导致细胞膜完整性破坏及炎症因子(如IL-1β、NLRP3、ASC)的大量释放。这一过程进一步加剧了局部神经炎症反应,并破坏神经元突触结构。通过使用CCR3特异性抑制剂SB328437或坏死性凋亡抑制剂Nec-1,可显著抑制星形胶质细胞的坏死性凋亡,减轻脑梗死体积,改善神经功能缺损。该成果系统揭示了趋化因子调控细胞程序性死亡的新机制,为开发靶向CCR3或坏死性凋亡通路的脑卒中治疗策略提供了重要的理论依据和实验基础。
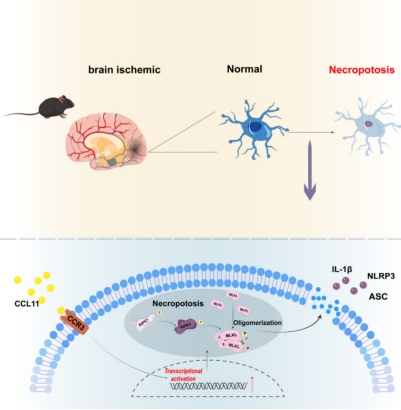
图注:脑缺血诱发坏死性凋亡机制示意图。
首先,CCL11特异性结合星形胶质细胞表面的CCR3受体并上调其表达。CCR3活化后引发坏死性凋亡的转录激活,随后磷酸化RIPK1诱导RIPK3发生磷酸化,进而促进磷酸化MLKL寡聚体的形成。这一过程最终导致细胞膜破裂及炎症因子(IL-1β、NLRP3和ASC)释放,从而加剧脑缺血后继发性损伤。
该研究得到国家自然科学基金和黑龙江省自然科学基金等项目的支持。论文第一作者为哈尔滨医科大学硕士研究生尹晗,王广友教授和张彤帅副教授作为共同通讯作者。
关键词:星形胶质细胞、CCL11、CCR3、坏死性凋亡、神经炎症、脑缺血
原文链接:DOI:10.1096/fj.202502723RR
通讯作者:
张彤帅,神经生物学教研室副教授,博士生导师,主要研究方向为缺血性脑卒中过程中免疫调控对中枢神经细胞及典型神经结构的影响及作用机制。主持国家自然科学基金1项,黑龙江省自然科学基金1项,黑龙江省博士后基金项目1项和其他省部级课题1项。发表SCI论文20余篇,其中第一作者/通讯作者7篇。获得黑龙江省科学技术奖二等奖1项。
第一作者:尹晗,现为哈尔滨医科大学基础医学院神经生物教研室硕士研究生,研究方向为脑缺血损伤调控神经细胞代谢重编程的作用及机制。
