近日,哈尔滨医科大学基础医学院神经生物学教研室王菁华教授团队在《Inflammation》期刊发表题为《Irgm1-Irf7 Axis Controls Macrophage Chemotaxis to Orchestrate Skeletal Muscle Regeneration》的研究论文。该研究首次揭示了免疫相关鸟苷三磷酸酶M1(Irgm1)在骨骼肌损伤修复中作为巨噬细胞趋化的核心开关,并阐明了其通过负向调控转录因子Irf7解除迁移抑制的分子机制。这一发现为治疗肌肉再生障碍性疾病提供了全新的依据和潜在治疗靶点。

研究发现,在小鼠氯化钡(BaCl2)诱导的急性骨骼肌损伤模型中,Irgm1的表达水平随损伤动态上调,且其表达动力学与巨噬细胞的浸润趋势高度平行。通过构建Irgm1髓系特异性敲除小鼠(Irgm1ΔCx3cr1)和肌纤维特异性敲除小鼠(Irgm1ΔHSA)证实,巨噬细胞来源的Irgm1,而不是肌肉来源的Irgm1对骨骼肌再生至关重要。Irgm1缺失会导致损伤处巨噬细胞招募显著减少,表现为炎症消退延迟、肌纤维再生受阻及功能恢复不全。相比之下,肌纤维特异性敲除Irgm1的小鼠则表现出正常的修复能力,明确了巨噬细胞是Irgm1发挥修复功能的关键细胞载体。
在机制层面,研究进一步证明Irgm1以细胞自主的方式调控巨噬细胞的趋化能力。Irgm1缺失会导致巨噬细胞对损伤信号的响应失灵,具体表现为关键趋化因子受体(如CCR1、CCR2和CCR5)的诱导性表达受挫。通过转录组测序筛查发现,Irgm1通过抑制干扰素调节因子7(Irf7)发挥作用。在Irgm1缺失的巨噬细胞中,Irf7异常蓄积并充当了迁移过程的“刹车”,而通过siRNA干预沉默Irf7可显著恢复巨噬细胞的迁移缺陷。该研究系统揭示了Irgm1-Irf7信号轴如何通过精细调控巨噬细胞的时空动态来协调骨骼肌修复进程。
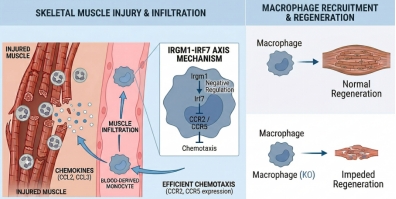
图注:Irgm1在骨骼肌损伤后通过抑制Irf7的异常积累,解除其对趋化因子受体CCR2和CCR5的转录抑制,从而确保巨噬细胞能够精准、高效地招募至损伤位点,启动后续的炎症消退与肌纤维再生进程。
关键词:骨骼肌再生、巨噬细胞、Irgm1、Irf7、趋化作用
原文链接:DOI:10.1007/s10753-026-02496-5
通讯作者:王菁华,哈尔滨医科大学基础医学院神经生物学教研室教授,博士生导师,中国神经科学学会理事,长期从事神经肌肉接头病和肌肉疾病的损伤修复与免疫调控机制研究。
第一作者:汪嘉麒,哈尔滨医科大学基础医学院神经生物学教研室博士研究生,师从王菁华教授,研究方向为骨骼肌损伤修复与免疫调控机制。
