2026年3月5日,哈尔滨医科大学基础医学院医学遗传学教研室、中国遗传资源保护与疾病防控教育部重点实验室孙文靖教授团队在染色体外DNA相关的研究中取得了重要的进展。相关研究成果以“KRAS-extrachromosomal DNA drives intratumoral heterogeneity in gastric cancer”为题,发表于国际肿瘤学领域重要期刊《Oncogene》(DOI: 10.1038/s41388-026-03713-z,JCR1区,中国科学院1区,IF7.3)。研究发现,KRAS-ecDNA在胃癌中可驱动肿瘤细胞的瘤内异质性,并通过多层次分子调控促进肿瘤进化。

胃癌是全球范围内发病率和死亡率均较高的恶性肿瘤之一,其发生发展过程中存在显著的肿瘤内异质性,这也是导致治疗抵抗和预后不良的重要原因。近年来研究发现,ecDNA(extrachromosomal DNA,ecDNA)是一类能够在细胞核中独立复制并携带癌基因的环状DNA结构。在多种肿瘤中发挥关键致癌作用。然而,ecDNA在胃癌中的具体功能及其调控机制仍有待深入研究。
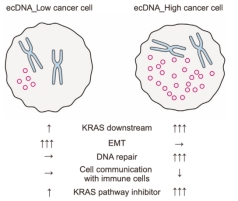
研究通过整合全基因组测序(WGS)和单细胞RNA测序(scRNA-seq)技术,对一例胃癌患者的肿瘤组织进行系统分析。研究团队首次在该患者中鉴定到携带完整KRAS基因的KRAS-ecDNA结构,并通过DNA-FISH等实验检测到其染色体外存在形式。进一步的单细胞转录组分析显示,KRAS-ecDNA可显著提高KRAS表达水平,并在肿瘤细胞中产生明显的表达差异,从而形成不同的功能亚群,揭示了ecDNA驱动肿瘤细胞异质性的分子基础。
在功能层面,研究发现ecDNA_High肿瘤细胞表现出更强的核糖体生物合成能力和DNA损伤修复活性,同时伴随特定转录因子调控网络的重编程。此外,该亚群细胞还呈现出MHC-II抗原呈递通路下调的特征,提示KRAS-ecDNA可能通过抑制免疫识别促进肿瘤免疫逃逸。这些结果表明,ecDNA不仅驱动癌基因扩增,还通过调控细胞增殖、基因表达和免疫相关通路,促进肿瘤的适应性进化。
在潜在治疗策略方面,研究团队利用计算生物学方法预测了不同肿瘤细胞亚群的药物敏感性。结果显示,KRAS-ecDNA_High细胞对MAPK信号通路抑制剂(如MEK或ERK抑制剂)以及部分上游受体酪氨酸激酶抑制剂具有较高敏感性,而对传统化疗药物则表现出普遍耐受性。这一发现提示,针对KRAS-ecDNA驱动的信号通路进行精准靶向干预可能成为胃癌治疗的新策略。
该研究从单细胞层面系统解析了KRAS-ecDNA在胃癌中的结构特征和功能作用,揭示了其在驱动肿瘤异质性、促进肿瘤进化以及影响治疗反应中的关键作用,为理解ecDNA介导的肿瘤生物学提供了新的证据,也为开发针对ecDNA驱动肿瘤的精准治疗策略提供了理论基础。
本研究得到国家自然科学基金、黑龙江省自然科学基金和哈尔滨医科大学少帅揭榜计划项目的支持。
第一通讯作者
孙文靖教授,哈尔滨医科大学星联教授,博士研究生导师。先后承担课题16项,包括“十四五”国家重点研发计划项目课题参加单位负责人1项,“十三五”国家重点研发计划项目子课题1项,国家自然科学基金3项,黑龙江省自然科学杰出青年基金1项,发表高质量学术论文80余篇。
共同通讯作者
傅松滨教授郝大鹏教授王浩副教授贾学渊副教授
第一作者
管荣,2025级博士研究生
李晨曦,2022级博士研究生
戴新纯,2023级博士研究生
